Règlement biocides, la lenteur du système européen

Temps de lecture estimé : 9 minutes
Il est lent, le Règlement biocides – RPB pour les intimes, BPR pour les anglophones et règlement (UE) nº 528/2012 pour les… rigoureux. Le programme d’examen des substances actives biocides dans l’Union européenne subit des retards considérables. Les délais de mise sur le marché des biocides s’allongent, notamment s’ils contiennent des substances actives qui n’ont pas encore été évaluées. Cependant, les dispositions du Règlement ont permis de faire face à la gestion des biocides pendant la pandémie, avec une demande sans précédent de désinfectants.
Par Hélene FRONTIER
Sommaire
Règlement biocides : accélérer le rythme
Huit ans après l’adoption du Règlement 528/2012, la Commission européenne (CE) a publié un rapport sur l’état d’avancement de sa mise en œuvre. Ce rapport couvre la période comprise entre le 1er septembre 2013 et le 31 décembre 2019.
Pour la CE, il est crucial d’achever le programme d’examen des substances actives pour atteindre les objectifs du Règlement biocides. En effet, plus il y a du retard, plus longtemps seront présents sur le marché des biocides contenant des substances actives dont la sécurité et l’efficacité n’ont pas encore fait l’objet d’une évaluation. Par conséquent, il est essentiel d’accélérer le rythme de l’évaluation des substances actives existantes et d’achever le programme d’examen dès que possible.
L’évaluation complète du Règlement sur les produits biocides (RPB), prévue pour 2025, analysera en profondeur l’adéquation du cadre réglementaire actuel comme base pour décider si des mesures supplémentaires sont nécessaires.
Les États membres doivent prendre les mesures nécessaires pour que leurs autorités puissent évaluer les demandes d’approbation, d’autorisation et de renouvellement. Si non, le système réglementaire défini dans le Règlement sur les produits biocides ne pourra pas fonctionner correctement.
Règlement biocides : où en est-on ?
Approbation des substances actives existantes dans le programme d’examen
Le programme de révision des substances actives existantes – celles qui étaient sur le marché au 14 mai 2000 – continue de subir des retards considérables, comme les années précédentes. Les principaux facteurs causant les retards sont :
- des ressources disponibles insuffisantes,
- des retards des demandeurs dans la transmission des données supplémentaires demandées par les États membres pendant l’évaluation,
- plusieurs questions techniques complexes concernant des dossiers spécifiques,
- l’évolution des orientations techniques,
- et l’adoption de nouveaux critères scientifiques pour les perturbateurs endocriniens.
Au 31 décembre 2019, seuls 35% des travaux liés au programme étaient terminés. Des décisions de la Commission ont été prises sur l’approbation ou la non-approbation de 252 combinaisons de substances actives avec des types de produits :
- 179 décisions ont été prises au titre du Règlement biocides ;
- 474 combinaisons de substances actives avec des types de produits sont encore à l’étude.
Entre 2014 et 2016, le nombre de décisions a régulièrement augmenté mais il a fortement diminué en 2017 et 2018.
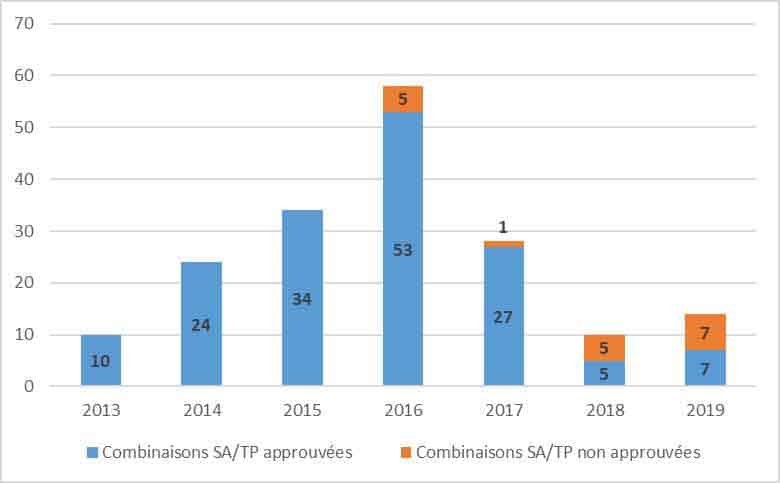
Nombre de combinaisons substance active/type de produit couvertes par les décisions d’approbation/non-approbation de la Commission | © Commission européenne (DR)
De nouvelles substances actives
L’innovation concernant les nouvelles substances actives biocides a été assez faible. En cause, des coûts réglementaires élevés et des procédures très longues, un marché des biocides réduit et fragmenté, ainsi que de faibles retours sur investissement. La lenteur du programme d’examen semble être également un frein supplémentaire.
Depuis l’entrée en vigueur du Règlement sur les produits biocides, seules dix nouvelles substances actives ont été évaluées. Sur ces 10 substances, 9 ont été approuvées, couvrant un total de 13 combinaisons de substances actives avec des types de produits.
Critères d’exclusion et de substitution
Des critères d’exclusion visent à supprimer progressivement les substances actives les plus dangereuses. Les substances répondant à ces critères ne peuvent pas être approuvées, sauf dérogation. Ces critères d’exclusion découragent les demandeurs d’autorisation de mise sur le marché d’introduire une demande de renouvellement de l’approbation de leur substance.
Sur 21 substances actives approuvées répondant aux critères d’exclusion, 9 sont des rodonticides. On estime qu’elles sont indispensables pour combattre un risque pour la santé humaine, pour la santé animale ou pour l’environnement en l’absence d’autres produits suffisamment efficaces.
Les critères de substitution visent quant à eux les substances particulièrement préoccupantes.
Autorisation de produit
En raison des retards du programme d’examen des substances actives, la majorité des produits biocides mis sur le marché (plusieurs dizaines de milliers) continuent de respecter la législation nationale, qui varie considérablement d’un État membre à l’autre. Dans beaucoup d’États membres, seule une notification est nécessaire pour commercialiser les produits. Dans d’autres États, il faut une autorisation.
Après l’approbation des substances actives qu’ils contiennent :
- près de 9 000 produits biocides sont autorisés,
- 6 400 ont été autorisés par des procédures de reconnaissance mutuelle,
- environ 2 600 ont fait l’objet d’une autorisation nationale indépendante.
Exceptions aux exigences d’autorisation
Entre 2014 et 2019, 9 États membres au total ont profité de cette possibilité. Ils ont accordé 135 autorisations temporaires pour des produits qu’ils jugeaient nécessaires. Cette situation a radicalement changé en 2020. Entre mars et novembre 2020, la Commission a reçu près de 600 notifications d’autorisations nationales. En effet, pratiquement tous les États membres ont utilisé cette disposition du Règlement biocides pour pouvoir commercialiser des désinfectants. Ces produits étaient nécessaires pour répondre à l’énorme demande qui a surgi pour contrôler la propagation du COVID-19.
La CE conclut que cette mesure d’urgence du Règlement a permis de faire face à la situation sans précédent provoquée par la pandémie de COVID-19.
Articles traités avec des biocides
Les contrôles effectués entre 2014 et 2018 ont indiqué qu’un nombre faible d’articles étaient traités avec des substances non autorisées. En revanche, les cas de non-conformité concernant les exigences d’étiquetage étaient plus nombreux. Au moins 30 % des articles examinés avaient une étiquette incorrecte ou incomplète.
Cas d’empoisonnement aux biocides
Le nombre total de cas enregistrés d’intoxications aux biocides varie de 5 248 en 2013 à 14 135 en 2018.
La majorité des cas d’empoisonnement seraient liés aux désinfectants (entre 47 et 59% des cas enregistrés annuellement) et aux produits antiparasitaires (entre 39 et 50%).
En termes de gravité des cas, le plus grand nombre de cas mortels ou quasi mortels (chez les humains ou les animaux autres que les animaux cibles) était lié aux produits antiparasitaires – contrôle des nuisibles.
La voie d’exposition la plus courante par laquelle des cas sont survenus est :
- l’ingestion, dans le cas des enfants ou des animaux de compagnie,
- et l’inhalation dans le cas des adultes.
La plupart des États membres ont pris des mesures pour éduquer et sensibiliser le grand public à l’utilisation des biocides et aux risques et avantages associés. Pour prévenir les cas d’intoxication, il est nécessaire de :
- encourager l’utilisation limitée des biocides,
- fournir des informations sur leur utilisation sûre.
Ceci est particulièrement vrai pour les désinfectants et les rodonticides,
Règlement biocides : le contexte
Pourquoi un Règlement sur les produits biocides ?
Les produits biocides sont potentiellement toxiques. Ainsi, leur utilisation et leur commercialisation doivent se faire conformément au Règlement (UE) nº 528/2012. Ce Règlement biocides en fixe les règles dans l’Union européenne (UE) depuis le 1er septembre 2013. Il a abrogé la directive 98/8/CE concernant la mise sur le marché des produits biocides. Son objectif est de garantir un haut niveau de protection de la santé humaine et animale et de l’environnement.
Rappelons tout de même que les biocides jouent un rôle important dans la protection de la santé publique. Par exemple, les insecticides et les désinfectants sont essentiels pour aider à contrôler par exemple :
- les maladies à transmission vectorielle,
- les maladies d’origine alimentaire,
- et les infections nosocomiales.
Le rôle déterminant des désinfectants est devenu particulièrement évident pendant la pandémie de COVID-19. En effet, ces produits sont désormais indispensables pour maitriser la propagation de la maladie.
Mise sur le marché depuis le RPB
Le Règlement biocides établit une approche en deux étapes :
- Les substances actives sont les ingrédients qui entrent dans la composition – également appelée formulation – des produits biocides. Ces substances doivent être :
- évaluées et approuvées au niveau de l’Union
- incluses à l’annexe I du RPB (liste des substances actives « à faible risque »).
Les substances actives sont approuvées pour des types de produits spécifiques.
- Ensuite, les produits biocides contenant ces substances actives nécessitent une autorisation pour leur commercialisation et utilisation dans l’UE. Cette autorisation se délivre au niveau national ou de l’Union. Il existe 22 types de produits biocides rassemblés dans quatre groupes principaux :
- désinfectants
- produits de protection
- produits de lutte contre les nuisibles
- autres produits biocides
Exceptionnellement, les produits biocides contenant des substances actives qui font partie du programme d’examen peuvent être mis sur le marché. On dit qu’ils sont en période transitoire. Il sera alors possible d’utiliser ces produits dans l’attente de la décision finale sur l’approbation des substances actives qu’ils contiennent.
Le Règlement sur les produits biocides prévoit également d’établir des exceptions :
- en cas de risque pour la santé humaine ou animale ou pour l’environnement,
- ou pour protéger le patrimoine culturel.
Cela permet aux États membres d’accorder des autorisations temporaires pour commercialiser des produits non autorisés.
lire également :







